5. Строение вещества
Мельчайшая частица вещества, имеющая все его химические свойства. Состоит из атомов.Молекула
Опыты, подтверждающие наличие промежутков между молекулами:
1. Растворение краски в воде: Растворим в стакане с водой небольшое количество краски. Отольем немного из стакана и дольем чистую воду. Жидкость стала светлее. Повторим процесс. Это доказывает, что между частицами, составляющими вещество, есть промежутки.
2. Тепловое расширение тел: Возьмем латунный шарик и кольцо, в которое он проходит. Начнем нагревать шарик. После нагревания шарик застрянет в кольце. После охлаждения снова пройдет. При нагревании расширяются не только твердые тела, но и жидкости. Это объясняется тем, что при нагревании промежутки между частицами увеличиваются, а при охлаждении - уменьшаются.
3. Расширение жидкости при нагревании: Закроем колбу пробкой и нальем жидкость в неё, отметив её уровень. Опустим колбу в горячую воду и увидим, как уровень жидкости повысится.
Поместим пластиковую бутылку в горячую воду. Через пару минут плотно закроем крышку. Достанем бутылку и остудим её. В результате бутылка деформируется и сохнется.
История развития атомной теории:
В V-IV веках до н.э. древнегреческие философы
Демокрит и Левкипп (V-IV вв. до н.э.)
Древнегреческие философы.
Предположили, что все состоит из неделимых и невидимых частиц - атомов.
От греч. "atomos" - неделимый.
Атом
Мельчайшая частица химического элемента.
От греч. "atomos" - неделимый.
Структурная единица вещества.
Благодаря трудам М.В. Ломоносова в XVIII веке представление о строении вещества достигло уровня научной теории.
Полное признание и развитие атомической теория получила в XX веке.
Пьер Гассенди (XVII век) предположил, что атомы отличаются друг от друга. Количество атомов составляет несколько десятков (118 атомов). Атомы могут образовывать небольшие устойчивые группы - молекулы.
Грубую оценку размеров молекул получил немецкий физик Вильгельм Рентген.
Определения:
Атом (гр. "неделимый") - мельчайшая частица химического элемента, структурная единица вещества.
Молекула - мельчайшая частица вещества, имеющая все его химические свойства.

Молекулы и атомы
Строение вещества
Молекулы одного и того же вещества одинаковы.
Диффузия:
Диффузия
Явление взаимного проникновения молекул одного вещества в промежутки между молекулами другого вещества.
Примеры: запах духов, окрашивание воды марганцовкой.
Скорость диффузии увеличивается с ростом температуры.
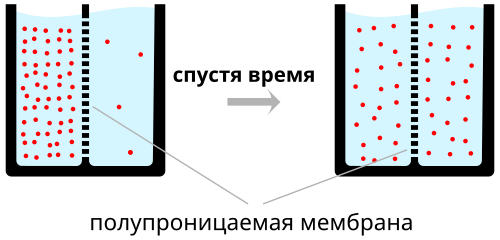
Диффузия
Процесс диффузии в жидкости
Примеры диффузии:
1. Духи - запах распространяется по комнате
2. Капля марганцовки в воде - вода окрашивается
3. Граница между брусками золота - золото проникает в серебро
Диффузия наблюдается и в твёрдых телах.
Скорость диффузии возрастает:
1. При увеличении расстояния между молекулами
2. При повышении температуры
3. При увеличении скорости движения молекул
В газах диффузия самая быстрая.
Важность диффузии в природе:
1. Всасывание корнями питательных веществ
2. Процесс питания и дыхания через листья
3. Аквариум и водоём снабжаются кислородом
4. Дыхание человека и животных
Броуновское движение:
Броуновское движение
Беспорядочное движение микроскопических частиц, взвешенных в жидкости или газе.
Открыто Робертом Брауном в 1827 году.
Объясняется ударами молекул по частице.
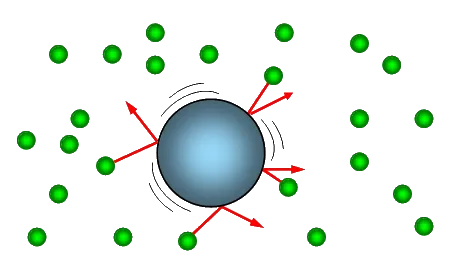
Броуновское движение
Хаотичное движение частиц
В 1827 году английский ботаник
Роберт Браун (1773-1858)
Английский ботаник.
В 1827 году открыл беспорядочное движение частиц пыльцы под микроскопом.
Это явление назвали броуновским движением в его честь.
Броуновское движение объясняется несбалансированным характером ударов молекул. Благодаря чему в каждый момент времени частица меняет своё направление движения и перемещается рывками.
Броуновское движение возможно не только в жидкостях, но и в газах.
Вопросы к уроку
1. Что такое атом и молекула? Чем они отличаются?
2. Приведи примеры опытов, доказывающих наличие промежутков между молекулами.
3. Что такое диффузия и броуновское движение? Почему они происходят?